Cell:兩項研究解析胚胎干細胞的表觀遺傳機制
來源:生物360
在干細胞研究領域中,表觀遺傳調控,尤其是細胞核內染色體高級組織形式一直是當前的前沿和熱點領域。近日,兩個研究小組在《細胞》(Cell)雜志上發表文章,分別報道了人類胚胎干細胞的轉錄和表觀遺傳動態機制 以及 多向分化胚胎干細胞的表觀遺傳作用機制。
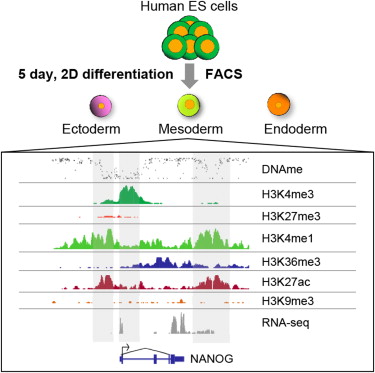
在第一項研究中,來自哈佛麻省Broad研究院,哈佛干細胞研究所等機構的科學家繪制出了關于人類胚胎干細胞三個胚層中細胞相關轉錄和表觀遺傳的全景圖。
人類胚胎干細胞(hESCs)分化過程是研究細胞轉換調控機制的一個獨一無二的模型,因此近年來以胚胎干細胞為模型,研究有關干細胞分化的表觀遺傳調控已成為新的研究熱點。
研究人員全面分析了人類胚胎干細胞三個胚層中直接定向分化的細胞,相關轉錄和表觀遺傳的特征,繪制出了一副重要的胚胎干細胞轉錄和表觀遺傳全景圖。
研究人員利用全基因組重亞硫酸鹽測序技術,并結合染色質免疫沉淀測序方法,以及RNA測序方法,揭示了與每個胚層細胞系特異性有關的中的特殊事件。在假設遠 端調控元件中出現了一些顯而易見的DNA甲基化和H3K4me1譜系特異性變化,而這些元件均頻繁的與未分化人類胚胎干細胞中多能性因子結合在一起。
而且研究人員也在未分化狀態的高DNA甲基化位點處,發現了胚層特異性H3K27me3的富集。
深入理解這些初始特異性事件,將有助于找到目前研究方法中的不足之處,從而發現更符合實際的分化策略,以及在細胞轉換過程中相關的調控機制。
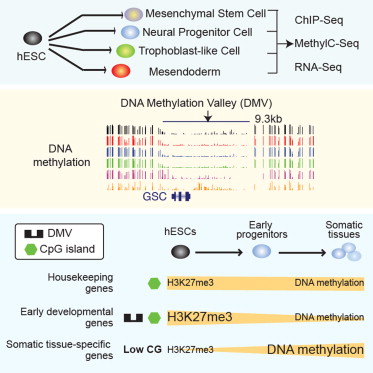
而在另一項研究中,研究人員全面分析了人類早期發育的基因表達機制,并發現了可能在胚胎遺傳和癌癥遺傳方面發揮重要作用的新的遺傳現象。公布的數據包括了超過四年的實驗分析,這將極大的幫助生物醫學幾乎每個子領域的研究工作。
研究人員發現在分析整個基因組的表觀遺傳組時,調節早期胚胎發育的主控基因往往由組蛋白甲基化H3K27me3關閉。同時,細胞分化的最后階段主要由DNA甲基化來精心安排,使細胞變得越來越專注于特定的功能。
人類基因組中有超過1200個大型的區域在發育過程中始終沒有DNA甲基化的存在。事實證明, 被認為是發育主控因子的許多基因都位于這些區域,研究人員稱它們為DNA甲基化谷(DNA methylation valleys, DMVs)。另外,研究人員還發現DMVs在結腸癌細胞中是異常甲基化的。我們知道,異常的DNA甲基化在多種癌癥中均發揮重要作用,這些結果暗示,細胞 DNA甲基化機制本身的改變可能是腫瘤發展的主要步驟。
這些研究數據將對科學界理解人類早期發展非常有用。這項研究的主要貢獻在于為生物醫學研究建立了一個主要的信息資源,許多復雜疾病的根源其實早就存在于人類早期發育的過程中。
原文檢索:
Casey A. Gifford, Michael J. Ziller, Alexander Meissner et al. Transcriptional and Epigenetic Dynamics during Specification of Human Embryonic Stem Cells. Cell, 09 May 2013; DOI: 10.1016/j.cell.2013.04.037
Wei Xie, Matthew D. Schultz, Bing Ren et al. Epigenomic Analysis of Multilineage Differentiation of Human Embryonic Stem Cells. Cell, 09 May 2013; DOI: 10.1016/j.cell.2013.04.022


