干細(xì)胞領(lǐng)域近期研究進(jìn)展匯總
干細(xì)胞是人體所有組織細(xì)胞的祖細(xì)胞、母細(xì)胞,是所有新生細(xì)胞的“生產(chǎn)基地”。大多時(shí)候,干細(xì)胞處于休眠狀態(tài),當(dāng)組織細(xì)胞遭受損傷時(shí)體內(nèi)干細(xì)胞就會被激活,出手相救。它們迅速產(chǎn)生大量的“子細(xì)胞”以替換修復(fù)受損的細(xì)胞、組織,從而實(shí)現(xiàn)組織、器官再造功能。
前兩天,“科學(xué)家首次在培養(yǎng)皿中利用干細(xì)胞培養(yǎng)出完美的人類血管”這一消息再次刷新干細(xì)胞領(lǐng)域研究技術(shù),震驚整個(gè)科學(xué)界。今天我們就整理下近期干細(xì)胞領(lǐng)域研究結(jié)果,供大家參考了解干細(xì)胞領(lǐng)域研究新進(jìn)展。
1、Cell Stem Cell:重大進(jìn)展!將人成熟的血細(xì)胞直接重編程為一類新的神經(jīng)干細(xì)胞
DOI:10.1016/j.stem.2018.11.015.
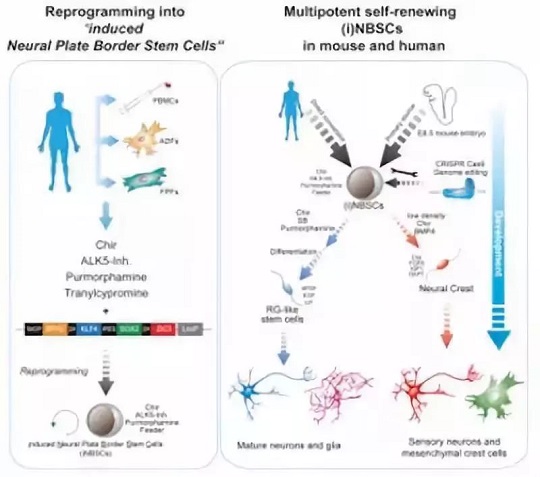
在一項(xiàng)新的研究中,來自德國癌癥研究中心(DKFZ)和海德堡干細(xì)胞技術(shù)與實(shí)驗(yàn)醫(yī)學(xué)研究所(HI-STEM)的研究人員首次成功地將人血細(xì)胞直接重新編程為一種以前未知的神經(jīng)干細(xì)胞。
這些誘導(dǎo)性干細(xì)胞類似于在中樞神經(jīng)系統(tǒng)的早期胚胎發(fā)育期間形成的干細(xì)胞。它們能夠在實(shí)驗(yàn)室中進(jìn)行修飾和無限期地增殖,并且代表著一種用于再生療法開發(fā)的候選對象。
相關(guān)研究結(jié)果于2018年12月20日在線發(fā)表在Cell Stem Cell期刊上,論文標(biāo)題為“Identification of Embryonic Neural Plate Border Stem Cells and Their Generation by Direct Reprogramming from Adult Human Blood Cells”。論文通訊作者為Andreas Trumpp和Marc Christian Thier。
2、PNAS:實(shí)錘!成年心臟并不存在心臟干細(xì)胞
DOI:10.1073/pnas.1805829115.
在一項(xiàng)新的研究中,荷蘭研究人員利用先進(jìn)的分子和遺傳技術(shù)構(gòu)建出在心肌梗塞發(fā)作之前和之后成年小鼠心臟中的所有分裂細(xì)胞的詳細(xì)細(xì)胞圖譜。他們得出結(jié)論:成年心臟不含有心臟干細(xì)胞。
在先前的研究中被鑒定為心臟干細(xì)胞的細(xì)胞最終產(chǎn)生血管或免疫細(xì)胞,但從未產(chǎn)生心肌。
相關(guān)研究結(jié)果發(fā)表在2018年12月26日的PNAS期刊上,論文標(biāo)題為“Profiling proliferative cells and their progeny in damaged murine hearts”。
3、Eur J Neurosci:經(jīng)過CRISPR/Cas9編輯的干細(xì)胞有望治療帕金森病
DOI:10.1111/ejn.14286.http://news.bioon.com/article/6731868.html
在英國,帕金森病的發(fā)病率大約為1/350。在一項(xiàng)新的研究中,來自英國愛丁堡大學(xué)和UCB制藥公司(UCB Pharma Ltd.)的研究人員在改善一種新出現(xiàn)的治療帕金森病的方法上邁出了關(guān)鍵一步。
這一進(jìn)展可能有助于開發(fā)一種有希望的稱為細(xì)胞替代療法(cell replacement therapy)的療法。專家們希望這種涉及將健康細(xì)胞移植到被帕金森病破壞的大腦區(qū)域中的療法能夠緩解震顫和平衡問題等癥狀。
相關(guān)研究結(jié)果近期發(fā)表在European Journal of Neuroscience期刊上,論文標(biāo)題為“Engineering synucleinopathy‐resistant human dopaminergic neurons by CRISPR‐mediated deletion of the SNCA gene”。
4、Cancer Cell:白血病復(fù)發(fā)的根源并不在于白血病干細(xì)胞而在于白血病再生細(xì)胞
DOI:10.1016/j.ccell.2018.08.007.
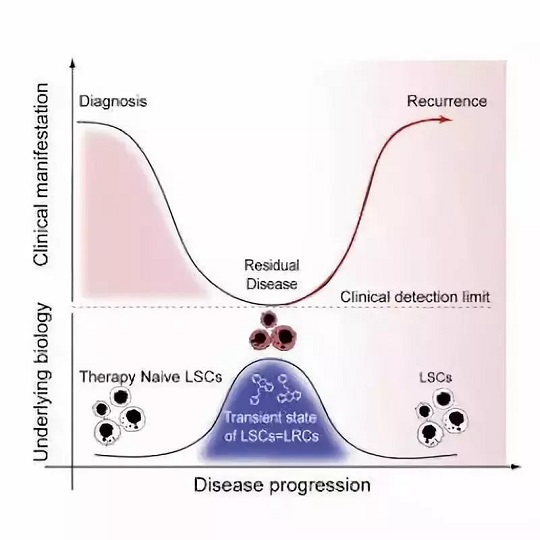
長期以來,癌癥研究人員一直認(rèn)為急性髓性白血病(AML)的復(fù)發(fā)是由于一群處于休眠狀態(tài)并且可能免受靶向分裂細(xì)胞的化療影響的白血病干細(xì)胞(LSC)。
然而,在一項(xiàng)新的研究中,加拿大麥克馬斯特大學(xué)的MickieBhatia及其同事們分析了患者樣本中的癌細(xì)胞群體以及從移植到小鼠體內(nèi)的AML白血病細(xì)胞中獲得的癌細(xì)胞群體,結(jié)果發(fā)現(xiàn)白血病干細(xì)胞在化療期間消失殆盡。
相關(guān)研究結(jié)果近期發(fā)表在CancerCell期刊上,論文標(biāo)題為“Identification of Chemotherapy-Induced Leukemic-Regenerating Cells Reveals a Transient Vulnerability of Human AML Recurrence”。
5、如何維持胚胎干細(xì)胞的無限潛能?
DOI:10.1038/s41467-018-07528-9

胚胎干細(xì)胞(ESCs)具有完全的潛能,其能夠轉(zhuǎn)化成為機(jī)體任何一種類型的細(xì)胞,一旦其開始沿著某一特定的路徑轉(zhuǎn)化成為某種特定的組織,胚胎干細(xì)胞就會失去無限的潛能,如今科學(xué)家們嘗試?yán)斫膺@一過程發(fā)生的方式和原因,旨在開發(fā)新型再生療法,即誘導(dǎo)機(jī)體自身的細(xì)胞替代受損或疾病的器官。
近日,一項(xiàng)刊登在國際雜志Nature Communications上的研究報(bào)告中,來自索爾克研究所的科學(xué)家們通過研究開發(fā)了一種新型蛋白復(fù)合體,其能抑制干細(xì)胞的發(fā)展,從而使其能夠維持無限的潛能。
這種名為GBAF的復(fù)合體或有望作為后期科學(xué)家們開發(fā)新型再生醫(yī)學(xué)療法的潛在靶點(diǎn)。
研究者Diana Hargreaves教授表示,這項(xiàng)研究中,我們始于對胚胎干細(xì)胞多能性的探索,這種多能性能夠促進(jìn)胚胎干細(xì)胞轉(zhuǎn)化成為機(jī)體中任何一種類型的細(xì)胞,闡明控制干細(xì)胞多潛能性的多種基因網(wǎng)絡(luò)非常重要。
因此能夠找到一種在這一調(diào)節(jié)過程中扮演關(guān)鍵角色的未知蛋白,對于研究者而言也是非常有意義的。
機(jī)體中的每一個(gè)細(xì)胞都有著相同的一套DNA元件,其包含有制造每一種可能性細(xì)胞類型的指令。
6、CellStemCell:震驚!高達(dá)10%的人體血細(xì)胞來自腸道中的造血干細(xì)胞庫
DOI:10.1016/j.stem.2018.11.007.
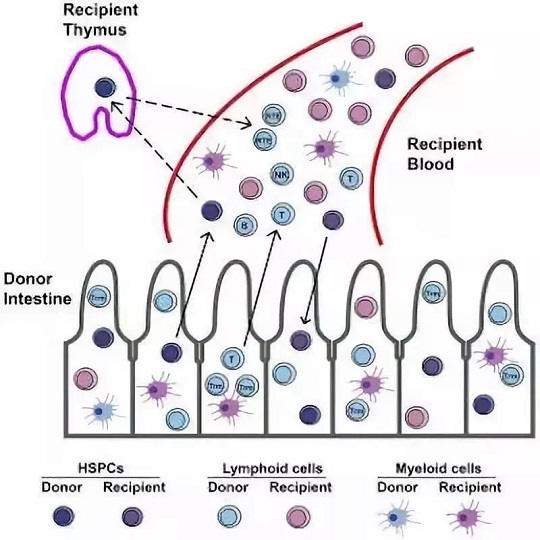
科學(xué)家們之前曾認(rèn)為血細(xì)胞是一群特殊的造血干細(xì)胞在骨骼中專門產(chǎn)生的。然而,在一項(xiàng)新的研究中,來自美國哥倫比亞大學(xué)瓦格洛斯內(nèi)外科醫(yī)生學(xué)會的研究人員吃驚地發(fā)現(xiàn)人體腸道可能利用它自身的造血干細(xì)胞庫提供高達(dá)10%的用于人體循環(huán)的血細(xì)胞。
相關(guān)研究結(jié)果于2018年10月29日在線發(fā)表在CellStemCell期刊上,論文標(biāo)題為“Human Intestinal Allografts Contain Functional Hematopoietic Stem and Progenitor Cells that Are Maintained by a Circulating Pool”。論文通訊作者為哥倫比亞大學(xué)的Megan Sykes。
為什么這項(xiàng)研究比較重要?
如果腸道發(fā)生功能障礙,那么腸道移植是患上克羅恩病和其他疾病的患者的唯一的長期治療選擇。但是較高的免疫排斥率和服用免疫抑制藥物時(shí)產(chǎn)生的危及生命的并發(fā)癥限制了人類腸道移植的成功率。
當(dāng)一個(gè)人接受移植器官時(shí),免疫系統(tǒng)通常將這種新移植的器官識別為外來物并加以破壞。強(qiáng)效的免疫抑制藥物可減輕這些反應(yīng),但是這會讓患者更容易受到感染和其他并發(fā)癥的影響。
7、Blood:科學(xué)家成功利用脂肪組織衍生的干細(xì)胞制造出人類血小板
DOI:10.1182/blood-2018-04-842641
近日,來自日本慶應(yīng)大學(xué)醫(yī)學(xué)院的科學(xué)家們開發(fā)出了一種新方法,其能在實(shí)驗(yàn)室促進(jìn)脂肪組織衍生的干細(xì)胞產(chǎn)生人類血小板,相關(guān)研究結(jié)果刊登于國際雜志Blood上,該研究表明,人工制造的血小板最終或能有效減少患者對血小板捐獻(xiàn)的依賴性,并幫助癌癥和其它疾病患者的康復(fù)。
血小板是機(jī)體血液中幫助凝血的一種關(guān)鍵組分,對于癌癥患者或進(jìn)行化療的患者、感染、免疫紊亂以及血小板紊亂的患者而言,輸血小板常常能夠挽救其生命。
每年全球大約有450萬單位的血小板被輸注,由于捐獻(xiàn)的血小板的保質(zhì)期不足一周時(shí)間,因此血小板的供應(yīng)常常無法滿足患者的需求,此外,由于供體的感染和受體出現(xiàn)的免疫反應(yīng),捐獻(xiàn)的血小板常常也會帶來潛在的安全風(fēng)險(xiǎn)。
這項(xiàng)研究中,研究人員基于此前的研究結(jié)果通過研究證實(shí),脂肪組織或能用來制造干細(xì)胞系,從而只需要12天就能夠產(chǎn)生正常功能的血小板。
8、新型干細(xì)胞療法有望徹底根治白血病
DOI:10.1126/scitranslmed.aat8410
干細(xì)胞移植能有效治療白血病,然而在很多情況下,來自供體的免疫細(xì)胞卻會攻擊受體患者機(jī)體的健康組織,從而產(chǎn)生致死性的后果。
近日,一項(xiàng)刊登在國際雜志Science Translational Medicine上的研究報(bào)告中,來自蘇黎世大學(xué)等機(jī)構(gòu)的科學(xué)家們通過研究鑒別出了一種在該過程中扮演關(guān)鍵作用的特殊分子,阻斷該分子的功能就能明顯改善接受干細(xì)胞移植療法患者的預(yù)后狀況。
干細(xì)胞療法能為白血病或骨髓癌癥患者完全康復(fù)帶來希望,這一療法需要去除患者因接受化療或放療所影響的細(xì)胞。
隨后利用健康供體機(jī)體中的血液干細(xì)胞來替代這些細(xì)胞,這些供體細(xì)胞能夠產(chǎn)生新的血細(xì)胞,并攻擊患者機(jī)體中的癌變細(xì)胞,從而抑制癌癥的復(fù)發(fā)。
注:文章內(nèi)容大部分來自生物谷公眾號


